Сабырқызы Анель – Алматы облысы
“Cаркан аудандық білім бөлімінің
К.Ушинский атындағы орта мектебі,
мектепке дейінгі шағын орталығымен”
Коммуналдық мемлекеттік мекемесінің химия пәні мұғалімі.
Сабақтың тақырыбы: Кристалдық торлар
Мақсаты:
Білімділік: оқушыларға молекулалық, атомдық және иондык кристалл торлары туралы түсінік беру, заттардың қасиеттері кристалл торлардың түріне байланысты екенін түсіндіру;
Дамытушылық: оқушылардың ой – өрісін, химия пәніне қызығушылығын арттыру, тұрмыста, еңбекте қолдану. Балалардың оқулықпен, қосымша әдебиетпен жұмыс жасау мүмкіндіктерін, қабілеттерін дамыту. Оқушылардың танымдық белсенділігін қалыптастыру.
Тәрбиелік: оқушыларды адамгершілікке, ұқыптылыққа, өз бетінше жұмыс істеуге баулу.
Көрнекі-құралдар:Интербелсенді тақта, электрондық оқулық, стикер, плакат, кристалды зат (мұз), шыны.
Сабақтың түрі: Саяхат сабақ.
Сабақтың әдіс-тәсілдері: мұғалімнің сөзі, кестемен, оқулықпен жұмыс, жеке және жалпы тапсырмалар, сұрақ – жауап әдісі.
Сабақтың барысы:
І Ұйымдастыру кезеңі аралы
-Оқушылармен амандасу;
-Оқушы санын түгелдеу;
-Оқушылардың эмоционалдық жағдайын тексеру, зейіндерін саббаққа аудару.
ІІ Үй тапсырмасын тексеру аралы: жазбаша үй жұмысына берілген қосылыстардың типін және ережелерін 3 оқушы тақтада актив студио бағдарламасы арқылы білімдерін тексеру. (сұрақтарға жауап беру)
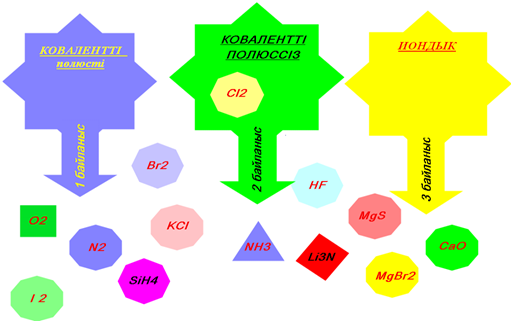
1. Электртерістілік дегеніміз не?
2. Байланыстың қанша түрі бар?
3. Коваленті полюсті байланыс?
4. Ковалентті полюссіз байланыс?
5. Ионды байланыс?
ІІІ «Жаңа сабақты түсіндіру» аралы.
Жаңа материалды түсіндіру.
КРИСТАЛДЫҚ ТОРЛАР
Көптеген қатты заттар кристалдық қүрылысты болады. Мүны оңай анықтауға болады. Кез келген қатты затты (қант, күкірт) ұсатып көріңдер. Олардың сынықтарынан белгілі пішіні бар кристалдарды оңай керуге болады. Мұндай заттарды кристалдық заттар деп атайды.
Қатты заттарды құраушы бөлшектердің кристалдық қүрылысы болатыны рентген сәулесінің көмегімен дәлелденген. Әр бір кристалдық заттарға жеке-жеке тоқталып түсіндіру.
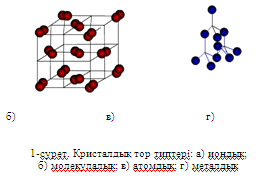
а) б) в) г)
1-сурет. Кристалдық тор типтері: а) иондык;
б) молекулалык; в) атомдык; г) металдык
Кристалдарда бөлшектер, иондар, атомдар немесе молекулалар геометриялык дұрыс ретпен белгілі бір аралықта орналасады. Осындай заңдылықпен орналасуы кезектесіп келетін бөлшектер тұрған тор кристалдық тор түйіндері деп аталады. Олар тордың құрылысына үқсайды, сондықтан ол кристалдық тор деп аталып, кристалдық заттың ішкі қүрылысын бейнелейді.
Қатты заттар өр түрлі геометриялық типтегі кристалдар түзеді. Байланыс типтеріне жөне болшек түрлеріне қарай кристалдық торлар: иондық, атомдық, молекулалық жөне металдық болып бөлінеді. 1-суретте кеңістікте орналасқан негізгі кристалдық тор типтері келтірілген.
ІV «Жаңа сабақты меңгеру» аралы
1. Бұл кезеңде оқушы тақтаға шығып, арнайы берілген кестені толтырып шығады.
Заттың
аталуы
Заттың формуласы
Химиялық байланыстың тип
Кристалдық
торы
Калий хлориді
Су қатты күйінде
Йод
Натрий хлориді
Кальций оксиді
Мыс
Көмірқышқыл газы
Көміртек (алмаз)
2. Кітапта тақырыптың соңындағы №4 есеп орындалады.
V «Жаңа сабақты бекіту» аралы
Сұрақ – жауап:
1. Кристалдық заттар дегеніміз қандай заттар?
2. Кристалдық тор және оның түйіндері дегенді қалай түсінесіңдер?
3. Иондық кристалдық тордың иондық кристалдық торынан айырмашылығы қандай?
4. Мына берілген гинетикалық есептерді шығарыңдар.
CaSO4 = CaO= CaCl2= Ca (OH)2= Mg(OH)2
Тренинг ойыны: «Сенесіз бе, сенбейсіз бе?»
Сенесіз бе, сенбейсіз бе, — Д.И.Менделеев 1869 жылы периодтық кестені ашты.
Сенесіз бе, сенбейсізбе, — Кальций оксиді коваленттік полюссіз байланысқа жататанына
Сенесіз бе, сенбейсіз бе, — NaH қосылысы ионды байланысқа жататынына
Сенесіз бе, сенбейсіз бе, — Азот элементінің электрондық формуласы мынаған тең болуына 1S2 2S 2 2p6 3S1
Сенесіз бе, сенбейсіз бе, — Магний элементінің атом құрамында 12протон,12 нейтрон, 12 электрон болуында;
VI Бағалау аралы: әрбір оқушыны өзінің сабаққа қатысқан белсенділігіне қарай бағалау
VІІ. Үйге тапсырма: §65 бет 170 Оқу.
Әр оқушы үш кристалдық тор түріне 5 мысалдан дайындап келу.
 sabaq.kz sabaq.kz
sabaq.kz sabaq.kz